Bereits 1766 entdeckte der englische Chemiker und Physiker Henry Cavendish bei seinen Experimenten mit Quecksilber und Säuren durch Zufall ein „neues" Gas: Wasserstoff. Wenn er gewusst hätte, dass das, was er da entdeckt hat, einige Jahrhunderte später eine wichtige Rolle in der Energiewende spielen würde ...
Wasserstoff: Der vielversprechendste Energieträger der heutigen Zeit
Wasserstoff ist der Hauptbestandteil der Sonnenmasse, das häufigste chemische Element im Universum, der Kraftstoff unserer Sonne und die Grundlage unseres Lebens.
Er kommt auf der Erde fast ausschließlich in Verbindung mit anderen Elementen vor – besonders mit Wasser und Biomasse.
Bei einer sehr geringen Dichte ist Wasserstoff gasförmig und hat pro Masse (kg) einen hohen Energieinhalt. Er ist ein gut geeigneter Energieträger für die chemische Langzeitspeicherung von elektrischer Energie
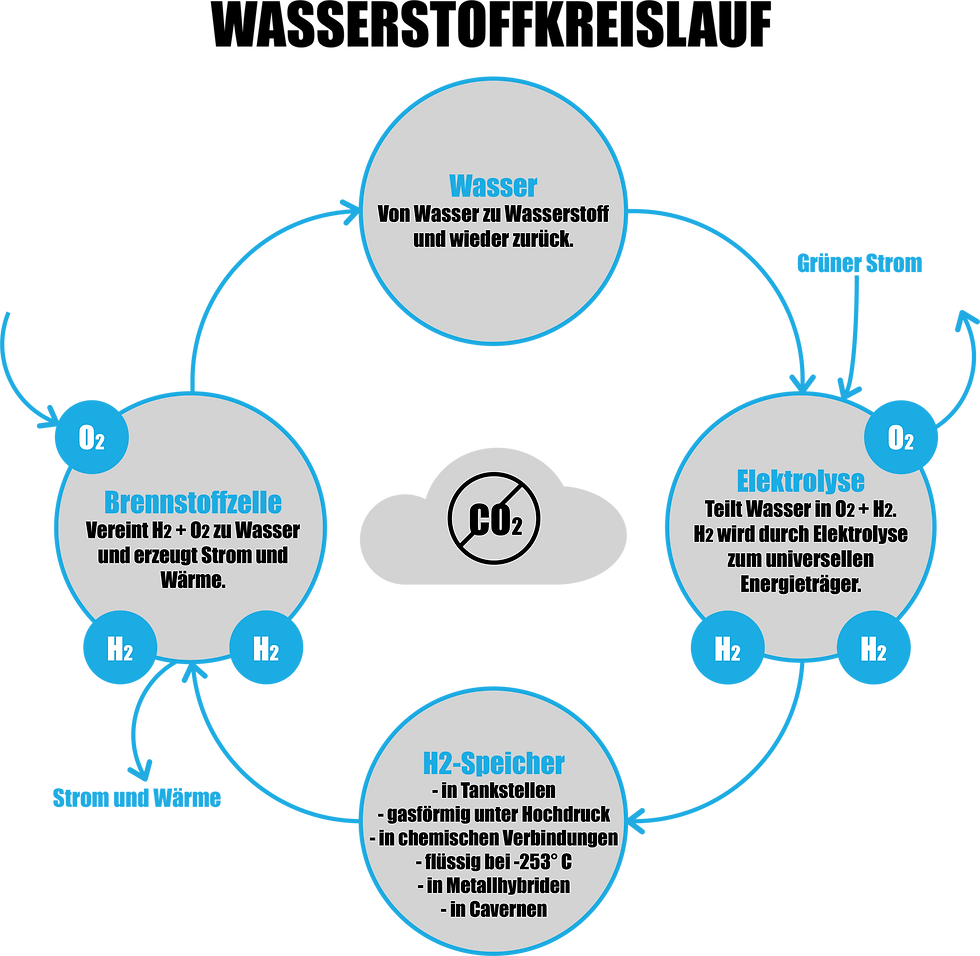
Verfahren zur Wasserstoffherstellung
Elektrolyse – die bekannteste und bewährteste Methode zur Wasserstoffherstellung
Bei der Elektrolyse wird mit Hilfe von elektrischem Strom destilliertes Wasser (H2O) in die Elemente Wasserstoff (H2) und Sauerstoff (O2) aufgespalten.
Es gibt zwei Hauptarten der Elektrolyse: die PEM (Proton Exchange Membrane) Elektrolyse und die alkalische Elektrolyse.
PEM = Proton Exchange Membran (Protonen-Austausch-Membran)
Die PEM-Elektrolyse zeichnet sich durch kurze Reaktionszeiten und ein hohe Stromdichte aus. Sie ist ausreichend teillastfähig und benötigt keinen Elektrolytkreislauf.
Die Membran ist das wichtigste Kennzeichen dieser Elektrolyse-Art. Sie trennt die Elektroden (Anode/Kathode) elektrisch voneinander und ist gleichzeitig auch gasdicht.
Beide Elektroden sind mit einem Katalysator belegt. Dieser sorgt für die Aufspaltung der Gasmoleküle (H2/O2), was unter Abgabe bzw. Aufnahme von Elektronen passiert.
An der Anodenseite wird Wasser zugeführt und in Sauerstoff sowie H+ aufgespalten. Die protonenleitende Polymer-Membran lässt die H+Protonen zur Kathodenseite diffundieren und verhindert, dass sich Wasserstoff und Sauerstoff vermischen.
Auf der Kathodenseite werden die Protonen mit Elektronen zu Wasserstoff kombiniert.
Teure Metalle wie Platin und Iridium werden als Katalysatoren verwendet.

AEL = Alkalische Elektrolyse
AEL ist das älteste Elektrolyse-Verfahren und weist damit eine fortgeschrittene Marktreife auf.
Es zeichnet sich durch eine hohe Langzeitstabilität aus und kommt ohne kritische und teure Rohstoffe aus. AEL hat eine relativ lange Kaltstartzeit und ist empfindlich gegenüber fluktuierenden Stromquellen.
Die Investitionskosten sind im Vergleich zu anderen Elektrolysesystemen relativ gering.
Die Aufspaltung des Wassers findet in hochkonzentrierten alkalischen Elektrolytlösungen (20 bis 40 % KOH) statt.
Im Kathodenraum entstehen dabei Wasserstoff und Hydroxid-Ionen. Diese werden durch die ionenleitfähige Membran auf die Kathodenseite geleitet. Dort reagieren Sie unter Elektrodenabgabe zu Sauerstoff und Wasser.
Die Membran arbeitet als Diaphragma und trennt den Anoden- und Kathodenraum. Sie ist gasundurchlässig und verhindert dadurch die Vermischung von Wasserstoff und Sauerstoff. Auf Grund ihrer Beschaffenheit verträgt sie keine Differenzdrücke und kann nur unter geringen Stromdichten (bis max. 600 mA/cm²) betrieben werden.
Typische Katalysatoren für die Elektroden sind eher preiswerte Materialien - basierend auf Ni, Co und Fe.
Die Aggressivität der hochkonzentrierten Elektrolyten führt dazu, dass in der Peripherie vor allem korrosionsresistente und teure Komponenten eingesetzt werden müssen.

Außerdem gibt es noch AEM (Alkalische-Austausch-Membran) - eine Kombination von PEM und AEL (Alkalische-Austausch-Membran).
Dampfreformierung – Wasserstoffherstellung aus Basis von Biogas
Die Dampfreformierung ist ein technisches Verfahren zur Herstellung von Wasserstoff.
In einem endothermen Prozess wird bei hohem Druck und hohen Temperaturen unter Verwendung eines Katalysators aus Bio-Methan und Wasser ein Synthesegas (Kohlenmonoxid und Wasserstoff) hergestellt.
In einem zweiten Prozessschritt wird das Kohlenmonoxid unter Zugabe von Wasserdampf in Kohlendioxid und Wasserstoff umgewandelt.
Bei diesem Prozess entstehen pro kg Wasserstoff ca. 10 kg CO2. Dieses kann aufgefangen und weiterverwendet werden, oder geht wie bei Verbrennungsprozessen in die Atmosphäre.
Hydrolyse – Aus Wasser werde Wasserstoff
Bei der Hydrolyse werden hauptsächlich biologisch Abfälle eingesetzt um bei ca. 180 °C Kohle und Dampf zu erzeugen.
Diese werden anschließend bei 1600 ° C in ein Synthesegas umgewandelt, aus dem der Wasserstoff separiert werden kann. Nach einer Reinigungsstufe kann dieser dann in der Mobilität in Brennstoffzellen oder Verbrennungsmotoren verwendet werden. Als weiteres Produkt entstehen Pflanzenkohle oder ähnliche Produkte.
Biologisch abbaubare Reststoffe aus der Landwirtschaft, Kommune und Industrie werden in kurzer Zeit in die hochwertigen Energieträger Bio-Kohle, Bio-Wasserstoff, Bio-Methanol und Bio-Methan umgewandelt.
Um einen 1 kg Wasserstoff herzustellen, werden ca. 15 kWh Energie benötigt.
Pyrolyse – Wasserstoffherstellung durch extreme Hitze
Bei der Pyrolyse wird Methan in Kohlenstoff und Wasserstoff zerlegt.
Diese Methode könnte damit eine Übergangslösung zur Wasserstofferzeugung sein, bei der noch fossile Energieträger verwendet werden.
In einem Flüssigmetall-Blasensäulenreaktor wird Methan durch die Metallschmelze (ca. 1000 ° C heißes Zinn) geleitet. Durch die hohe Temperatur wird das Methan in seine atomaren Bestandteile zersetzt. Der Kohlenstoff setzt sich aufgrund seiner Dichte oberhalb der Zinnschmelze ab. Er liegt dabei in Pulverform vor. Der gasförmige Wasserstoff wird oberhalb der Schmelze gesammelt und anschließend gereinigt. Er wird farblich als „türkiser Wasserstoff“ betrachtet.
Für die Gewinnung von Wasserstoff mittels Pyrolyse wird nur ein Fünftel der Energie benötigt, die man für die Gewinnung derselben Menge Wasserstoff mittels Elektrolyse aufwenden muss.
Plasmalyse – Wasserstoffherstellung mit ionisiertem Gas
Die Plasmalyse ist wie die Elektrolyse ein elektrochemisches Verfahren, bei dem im hochfrequenten oder Gleichstrom- Plasmafeld Wasserstoff und andere Industriegase erzeugt werden.
Sie kann u.a. für die Bearbeitung von Schmutzwasser oder Schlammwasser eingesetzt werden. Die Methan-Plasmalyse erzeugt Wasserstoff und Carbon Black.
Sie bietet damit die Möglichkeit der dezentralen Dekarbonisierung von Erdgas bzw. bei Verwendung von Biogas auch die Realisierung einer aktiven verfahrenstechnischen CO2-Senke.
Zur Erzeugung von Wasserstoff werden bei Schmutzwasser ca. 20 kWh und bei Methan ca. 10 kWh Energie pro kg H2 benötigt.
Was ist denn jetzt die beste Methode zur Wasserstoffherstellung?
Wir persönlich sind große Fans der PEM-Elektrolyse und der Dampfreformierung.
ABER: Die Effizienz eines Verfahrens zur Wasserstoffherstellung hängt von verschiedenen Faktoren ab, einschließlich der Energieeffizienz, der Umweltverträglichkeit, der Skalierbarkeit und der Kosten. Es gibt kein einzelnes Verfahren, das in jeder Hinsicht überlegen ist, da jedes Verfahren Vor- und Nachteile hat und für verschiedene Anwendungen geeignet sein kann.
„Das Wasser ist die Kohle der Zukunft. Die Energie von morgen ist Wasser, das durch elektrischen Strom zerlegt worden ist. Die so zerlegten Elemente des Wassers, Wasserstoff und Sauerstoff, werden auf unabsehbare Zeit hinaus die Energieversorgung der Erde sichern.“
―Jules Verne

Commentaires